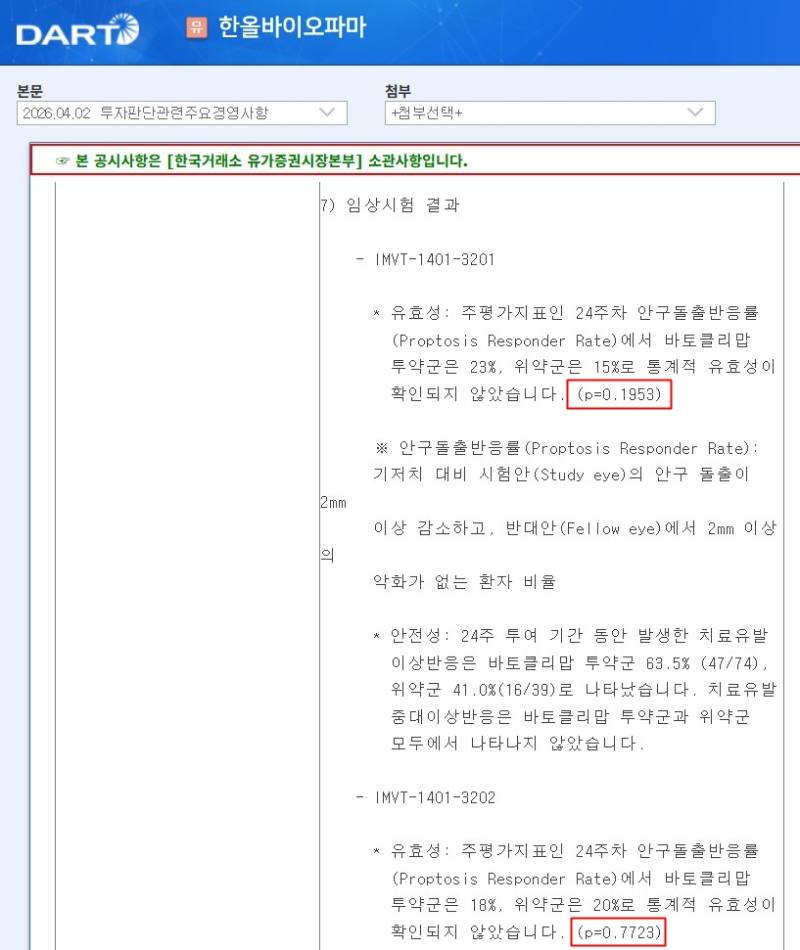
한올바이오파마의 바토클리맙 TED 임상 3상 결과 공시 (자료=금융감독원 전자공시시스템)
◇한올바이오 '바토클리맙' TED 임상 3상 2건 '실패'
한올바이오파마의 파트너사 이뮤노반트(Immunovant)는 최근 '바토클리맙'의 TED 임상 3상 결과를 발표했다. 이뮤노반트는 해당 임상 3상을 IMVT- 1401 -3201(3201 임상)과 IMVT -1401 -3202(3202 임상)로 2건을 진행다. 톱라인 결과 모두 1차평가지표를 미충족한 것으로 나타났다. 3201 임상은 p값 0.1953으로 통계적 유의성이 없었다. 3202 임상은 p값이 0.7723이라 위약보다도 못한 결과가 도출됐다.
이뮤노반트는 현재 차세대 FcRn 억제제 'IMVT-1402'을 다양한 자가면역질환 적응증을 대상으로 임상개발하는데 집중하고 있다. 특히 그레이브스병을 핵심 전략 적응증으로 설정, IMVT-1402의 그레이브스병 임상의 톱라인 데이터를 내년에 발표할 예정이다.
이뮤노반트 측은 "파트너사 한올바이오파마와 함께 바토클리맙의 향후 개발 계획을 검토할 예정"이라며 "추후 공동으로 업데이트를 제공할 계획"이라고 밝혔다. 앞서 이뮤노반트는 지난해 12월 바토클리맙의 권리 일부를 한올에 반환하기 위해 논의를 시작했다고 밝혔다.
앞서 아제넥스도 FcRn 억제제인 에프가르티기모드(efgartigimod)를 기반으로 TED 임상을 추진했지만 사실상 개발을 중단했다. 일부 지표에서 유효성 신호가 관찰됐지만 안구돌출 개선 효과가 기대에 못 미쳤기 때문으로 풀이된다. TED 신약 승인을 결정짓는 핵심 지표는 안구돌출 개선 효과로 FDA 허가를 받은 테페자(Tepezza)는 평균 2~3㎜ 수준의 안구돌출 감소 효과를 입증했다.
바이오업계에서는 이번 한올바이오파마 사례와 맞물리며 FcRn 기전의 TED 치료제 개발이 한계에 부딪힌 것 아니냐는 우려가 나오고 있다. 두 신약후보물질 모두 FcRn 기전으로 TED 적응증에 접근했지만 결과적으로 유의미한 치료 효과를 입증하지 못했기 때문이다.
바이오업계 관계자는 "FcRn이 전신 자가면역질환에서는 유효할 수 있다"며 "하지만 TED처럼 국소 조직 변화가 중요한 질환에서는 효과가 제한적인 게 아닌가 싶다"고 추정했다.
◇FcRn 한계에 CD40L 대안 부상…'APB-A1'에 관심 쏠려
이러한 흐름 속에서 투자자들의 관심은 자연스럽게 대체 기전을 가진 에이프릴바이오로 이동하고 있다. 에이프릴바이오는 CD40L을 타깃으로 하는 자가면역치료제 'APB-A1'을 보유하고 있다. FcRn 억제제가 이미 생성된 항체를 제거하는 방식이라면 CD40L 저해제는 항체 생성 자체를 차단하는 방식이지만 심혈관계 부작용 문제가 제기돼 왔다.
에이프릴바이오는 파트너사 룬드벡을 통해 APB-A1의 TED 임상 1b상을 진행하고 있다. APB-A1은 임상 1b상 첫 중간 분석에서 안구 돌출(proptosis)이 임상적으로 의미 있는 기준으로 여겨지는 2㎜ 이상 개선되는 결과를 보였다. 소규모 환자군 기반 중간 분석이지만 초기 데이터에서 일부 환자군을 대상으로 유의미한 개선 신호가 확인되면서 CD40L 기전의 치료 가능성을 탐색할 수 있는 근거를 확보했다는 평가가 나온다.
APB-A1의 최종 임상 1b상 데이터는 오는 6월 13일부터 16일까지 미국 시카고에서 열리는 세계 내분비학회(ENDO 2026)에서 공개될 예정이다. 룬드벡은 ENDO에서 APB-A1의 안구 돌출 개선 효과의 지속성, 안전성 등에 대한 상세한 데이터를 발표할 것으로 전망된다.
해당 데이터를 통해 APB-A1의 임상적 경쟁력을 가늠할 수 있을 것으로 예상된다. 특히 룬드벡은 이미 APB-A1의 임상 2상을 연내 개시하기로 결정한 상태다. 임상 1b상 결과를 최종 확인하기 전에 후속 임상 개시를 결정한 것이다.
바이오업계 관계자는 "임상 1상 완료 전 임상 2상 진입을 결정한다는 게 반드시 임상 1상이 성공했다는 의미는 아니다"라면서도 "중간 데이터에서 긍정적인 신호를 확인했기 때문에 개발 속도를 높였을 것이라는 추론은 어느 정도 가능하다"고 언급했다.
룬드벡이 APB-A1의 적응증 확장을 계획하고 있다는 점도 이번 임상을 통해 유효성 신호를 확인할 것이라는 기대감이 반영된 것으로 보이는 대목이다. 룬드벡은 APB-A1이 TED를 시작으로 △다발성경화증 △중증근무력증 △시신경척수염 △프리드리히 운동실조증 등 다양한 신경면역질환으로 확장 가능성이 있다고 보고 있다.
위해주 한국투자증권 연구원은 "APB-A1의 TED 환자 대상 중간 결과는 단일 용량군임에도 임상적으로 의미 있는 안구돌출 감소를 보였다"며 "추가적인 효능 개선 여지가 크다고 판단하며 부작용 프로파일 측면에서 테페자 비교 우위일 것"이라고 말했다. 이어 "임상 결과에 따른 에이프릴바이오의 재평가는 이제 시작에 불과하다"고 내다봤다.










